-
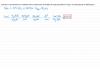
Como seria la solucion de esto? Gracias

-
Hola, como seria el siguiente ejercicio:
Indique los posibles valores de los tres primeros números cuánticos correspondientes a los orbitales 2p y 4d.
Tendría que poner las 6 combinaciones distintas de los electrones del orbital 2p y en el caso del 4d las 10?
-
Estoy haciendo química orgánica y tengo dudas con este en concreto, ya que no sé si el hepta se sitúa antes o después del ciclo, podrían ver mi respuesta e indicarme si está bien y si no, que debo hacer, Muchas gracias.