-
 Buenas noches. Asunto: 3ºESO, peróxidos, simplificación y nomenclatura. Mi libro tiene algunos errores respecto al asunto. ¿Por favor me podéis confirmar si es correcto lo describo en el documento anexo, lo cual resumo brevemente a continuación?Gracias.
Buenas noches. Asunto: 3ºESO, peróxidos, simplificación y nomenclatura. Mi libro tiene algunos errores respecto al asunto. ¿Por favor me podéis confirmar si es correcto lo describo en el documento anexo, lo cual resumo brevemente a continuación?Gracias.En la simplificación y nomenclatura del peróxido de platino (IV) entiendo que lo más aconsejable es formularlo como PtO4, en lugar de dejar constancia expresa del ión peróxido (O2) y los subíndices [Pt2(O2)4]. En cuanto a la nomenclatura de este compuesto entiendo que, salvo error, sólo caben dos, a saber, tetraóxido de platino y peróxido de platino (IV), ya que creo que no corresponde nombrarlo con el valor de la carga iónica toda vez que el compuesto no tiene carácter iónico.
Respecto a la fórmula del peróxido de hierro (II) (FeO2) planteo la misma duda respecto a la simplificación. Es decir, describirla tal como acabo de indicar. En la nomenclatura de composición, sí caben las tres denominaciones (prefijos multiplicadores, número de oxidación y valor de la carga iónica. Aunque en este último caso no estoy seguro de que la que mi libro describe sea correcta: Dióxido (2-) de de hierro (2+). En el adjunto documento describo otra posibilidad de denominación según la carga iónica (por supuesto tampoco estoy totalmente seguro de mi alternativa. He mirado al respecto las nuevas reglas de la IUPAC (ya no tan nuevas, realmente) y no soy capaz de saber qué corresponde.
-
Hola! Necesito ayuda con este ejercicio, me he quedado bloqueada (3ºESO). Gracias de antemano :)
(No pretendo que me hagan la tarea, solo quiero entenderlo)


Jerónimo
el 31/3/19Primero ajusta la reacción ,si estas en 3º imagino que lo harás por tanteo o algebraicamente, ya tendrás las relaciones molares entre reactivos y productos
Estequiometria 01 -
Se intenta oxidar Cobre metálico por reacción con ácido nítrico (HNO3)
Me piden que ponga las semirreacciones de oxidación y reducción:
He visto la solución, pero no entiendo porque en la reacción de reducción se utiliza el NO3 que pasa a ser NO, en vez de utilizar el HNO3
-
Alguien me podria ayudar? No se como empezar
Se introducen 245.14 g de un gas ideal de fórmula X2 en un recipiente vacío, con paredes diatérmicas y separado del exterior por un émbolo móvil. Cuando la presión atmosférica
es de 766.4 mmHg y la temperatura exterior es de 33.15 ° C, el gas ocupa un volumen aproximado de unos 161 L. Determinar qué gas se ha introducido y calcular el volumen exacto.


Jerónimo
el 30/3/19Aplicas PV=nRT para sacar la masa molar aproximada n=PV/RT =(1,008*161)/(0,082*306,15)=6,46 moles n=g/Mm Mm=245,14/6,46=37,90 g/mol
Buscando las masa molares de los gases vemos que el que más se aproxima a nuestro resultado es el Cl2 de valor 35,45 g/mol
Vuelves a aplicar PV=nRT con el valor exacto del Cl2 y despejas el volumen exacto.
-
Hola! Buenas noches, una pregunta, ¿qué es lo que pasa si la capacidad de desabsorción de un compuesto es mayor a la de absorción? Gracias


Breaking Vlad
el 30/3/19Hola Sol,
Sentimos informarte de que en www.unicoos.com no resolvemos dudas de nivel universitario. Contestamos dudas que estén directamente relacionadas con el contenido de los vídeos.
Un saludo,
Breaking Vlad





















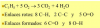
 No entiendo porque se pone c ( 1-alfa . No sería x -1
No entiendo porque se pone c ( 1-alfa . No sería x -1





